La complexitat de cèl·lules i teixits que formen un cos animal parteix d’una bola enganyosament simple de cèl·lules mare embrionàries (CME), l’embrió primerenc. La forma en què aquestes cèl·lules perden la seva pluripotència (és a dir, la seva capacitat per donar lloc a qualsevol tipus de cèl·lula) i com es diferencien en llinatges específics és un dels misteris de la biologia del desenvolupament. Un misteri sobre el qual el grup de recerca dirigit per Thomas Graf al Centre de Regulació Genòmica (CRG) hi ha aportat llum.
L’embrió vertebrat comença com una esfera uniforme de cèl·lules pluripotents que aviat es transforma –a través d’un procés anomenat gastrulació– en una estructura més complexa amb tres capes de tipus cel·lulars diferenciats. Aquestes tres capes germinals s’anomenen Endoderm (capa interna), Mesoderm (capa mitjana) i Ectoderm (capa externa) i donaran lloc a totes les cèl·lules i teixits de l’organisme adult.
- Endoderm (capa interna) → tractes digestiu i respiratori
- Mesoderm (capa mitjana) → muscles, òssos i dermis
- Ectoderm (capa externa) → espidermis, cabell, ungles, ulls, i sistema nerviós
Les tres capes germinals de l’embrió – Endoderm, Mesoderm i Ectoderm – donaran lloc a totes les cèl·lules i teixits de l’organisme adult.
Es pensava que el mecanisme pel qual les cèl·lules mare embrionàries (CME) perden el seu estat pluripotent, i comencen a diferenciar-se en capes germinals específiques era un procés de 2 passos:
- Primer, sortida de pluripotència → Les CME perden la capacitat per convertir-se en qualsevol tipus de cèl·lula. A nivell molecular, això passa degut a la inhibició dels gens Oct 4, Sox 2 i Nanog.
- Segon, especificació del llinatge → Les CME es diferencien en cèl·lules de l’ectoderm, el mesoderm o l’endoderm. A nivell molecular això succeeix activant un grup específic de gens per a cada capa:
- Gata4 i Brachyury (T) en el cas del mesoderm.
- Gata6, Foxa2 i Sox17 en el cas de l’endoderm.
- Pax6 i Sox1 en el cas de l’ectoderm.
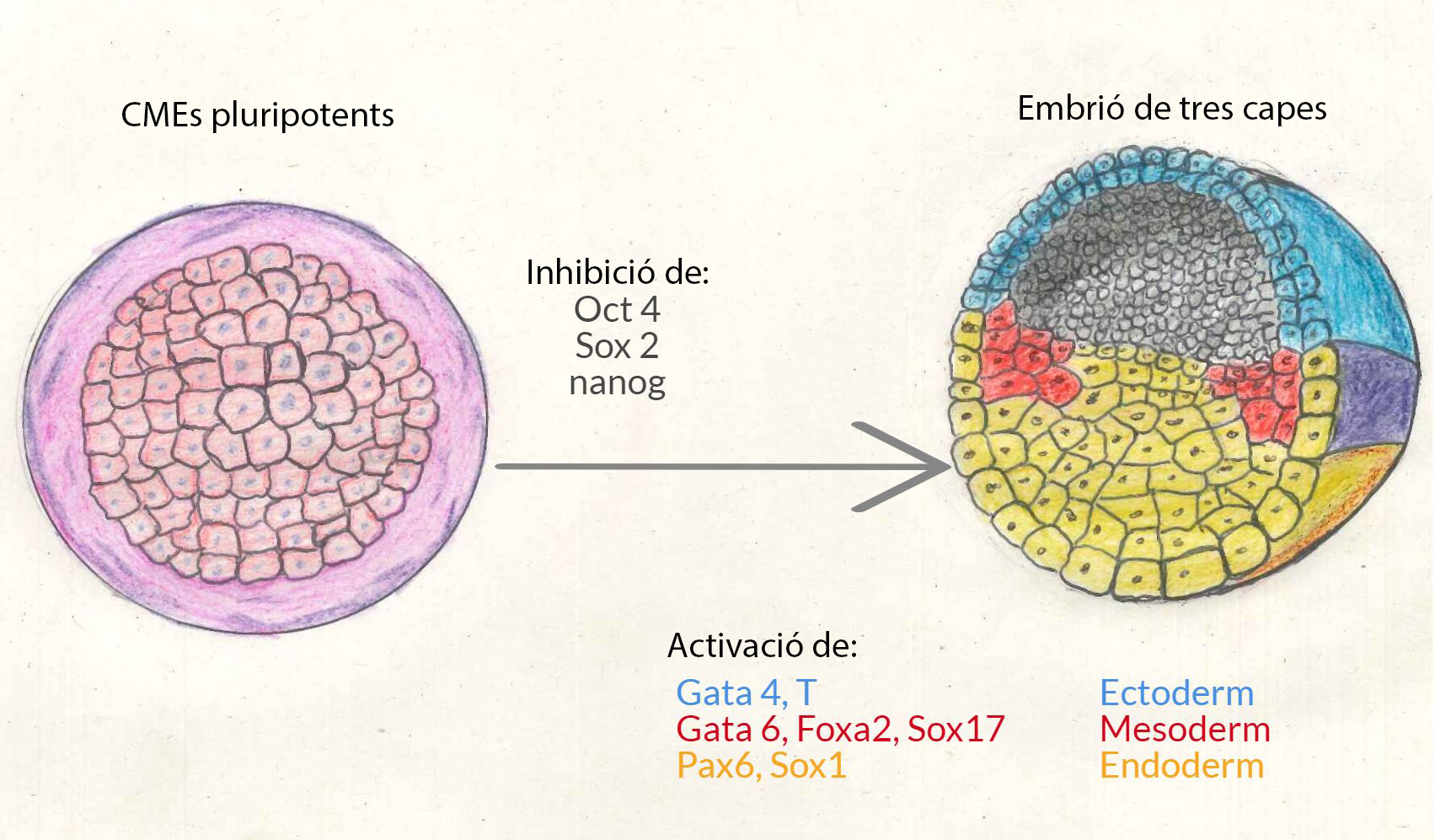
La inhibició i l’activació d’aquests grups de gens fa que la cèl·lula passi d’una cromatina relativament oberta (quan la cèl·lula és pluripotent) a una de més compactada (quan la cèl·lula es diferencia).
Ara, Tian Tian i altres companys del laboratori Graf del CRG, han trobat que la sortida de pluripotència i l’especificació de la capa germinal es poden sobreposar, en lloc de passar una després de l’altra, i han descobert alguns actors crítics del procés. En particular, els científics es van centrar en el factor Whsc1 relacionat amb la cromatina, una histona metilasa que s’ha associat a una forma rara de malaltia genètica i a la formació del mieloma múltiple. Els investigadors van trobar que:
- Quan s’inhibeix Whsc1, les cèl·lules mare embrionàries del ratolí no es poden diferenciar de manera eficient en cèl·lules del mesendoderm (encara que no es vegi afectat l’ectoderm), i la sortida de pluripotència es retarda. Això fa que Whsc1 sigui el primer factor relacionat amb la cromatina que es demostra que era necessari per a la sortida de la pluripotència.
- Whsc1 és un enzim que pot metilar la histona. Tot i això, la funció de Whsc1 en la sortida de pluripotència i la diferenciació del mesendoderma és independent del seu domini catalític, i per tant d’aquesta funció.
- Whsc1 s’uneix al elements reguladors dels gens ‘mestres’ de llinatge Gata4, T (Brachyury), Gata6 i Foxa2 i els activa, donant lloc a una especificació de cèl·lules germinals. Això ho fa juntament amb Brd4.
Els autors conclouen que Whsc1 vincula el silenciament de la xarxa reguladora de pluripotència amb l’activació dels llinatges del mesendoderm i, per tant, juga un paper clau en aquesta important transició a l’embrió.
El laboratori dirigit per Thomas Graf ha trobat que el factor relacionat amb la cromatina Whsc1 juga un paper clau en la diferenciació de l’embrió primerenc; enllaça la sortida de pluripotència amb l’especificació del llinatge del mesendoderma.
“El nostre descobriment anul·la l’antic concepte que les cèl·lules pluripotents han d’oblidar primer qui són abans que puguin aprendre noves regles que els permetin canviar d’identitat. Per què i com Whsc1 només estableix una connexió amb dues de les tres capes germinals és una qüestió interessant per al futur ”, diu Thomas Graf, líder d’aquest estudi, fet en col·laboració amb la Universitat Harvard, l’Institut Whitehead per a la Recerca Biomèdica i el MIT a Cambridge, EUA.
En aquest vídeo (en anglès) Thomas Graf ens explica aquesta recerca.
Tian V. Tian et al. Whsc1 links pluripotency exit with mesendoderm specification. Nat Cell Biol. 2019 Jul;21(7):824-834. doi: 10.1038/s41556-019-0342-1. Epub 2019 Jun 24.