La complejidad de células y tejidos que forman un cuerpo animal parte de una bola engañosamente simple de células madre embrionarias (CME), el embrión temprano. La forma en que estas células pierden su pluripotencia (es decir, su capacidad para dar lugar a cualquier tipo de célula) y como se diferencian en linajes específicos es uno de los misterios de la biología del desarrollo. Un misterio sobre el cual el grupo de investigación dirigido por Thomas Graf en el Centro de Regulación Genómica (CRG) ha aportado luz.
El embrión vertebrado empieza como una esfera uniforme de células pluripotentes, que pronto se transforma –a través de un proceso denominado gastrulación– en una estructura más compleja con tres capas de tipos celulares diferenciados. Estas tres capas germinales se denominan Endodermo (capa interna), Mesodermo (capa mediana) y Ectodermo (capa externa) y darán lugar a todas las células y tejidos del organismo adulto.
- Endodermo (capa interna) → aparato digestivo y respiratorio
- Mesodermo (capa mediana) → músculos, huesos y dermis
- Ectodermo (capa externa) → epidermis, pelo, uñas, ojos y sistema nervioso
Las tres capas germinales del embrión – Endodermo, Mesodermo y Ectodermo – darán lugar a todas las células y tejidos del organismo adulto.
Hasta ahora se creía que el mecanismo por el cual las células madre embrionarias (CME) pierden su estado pluripotente, y empiezan a diferenciarse en capas germinales específicas era un proceso de 2 pasos:
- Primero, salida de pluripotencia → Las CME pierden la capacidad para convertirse en cualquier tipo de célula. A nivel molecular, esto pasa debido a la inhibición de los genes Oct 4, Sox 2 y Nanog.
- Segundo, especificación del linaje → Las CME se diferencian en células del ectodermo, el mesodermo o el endodermo. A nivel molecular esto sucede activando un grupo específico de genes para cada capa:
- Gata4 y Brachyury (T) en el caso del mesodermo.
- Gata6, Foxa2 y Sox17 en el caso del endodermo.
- Pax6 y Sox1 en el caso del ectodermo.
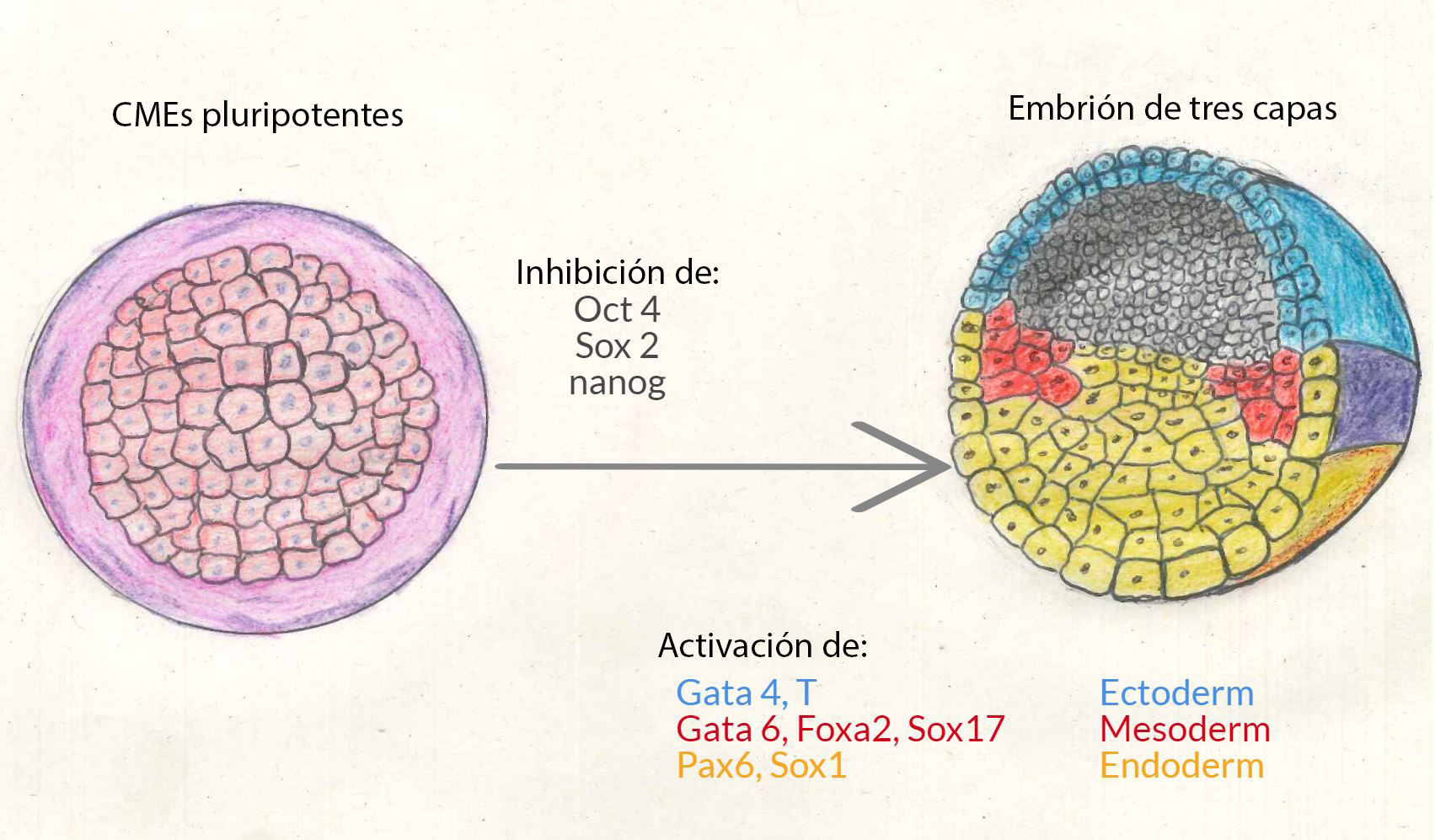
La inhibición y la activación de estos grupos de genes hace que la célula pase de una cromatina relativamente abierta (cuando la célula es pluripotente) a una más compactada (cuando la célula se diferencia).
Ahora, Tian Tian y otros compañeros del laboratorio Graf del CRG, han encontrado que la salida de pluripotencia y la especificación de la capa germinal se pueden sobreponer en el tiempo, en lugar de pasar una después de la otra, y han descubierto algunos actores críticos del proceso. En particular, los científicos se centraron en el factor Whsc1 relacionado con la cromatina, una metilasa de histonas que se ha asociado a una forma rara de dolencia genética y a la formación del mieloma múltiple. Los investigadores encontraron que:
- Cuando se inhibe Whsc1, las células madre embrionarias del ratón no se pueden diferenciar de manera eficiente en células del mesendodermo (aunque no se vea afectado el ectodermo), y la salida de pluripotencia se retrasa. Esto hace que Whsc1 sea el primer factor relacionado con la cromatina que se ha demostrado que es necesario para la salida de la pluripotencia.
- Whsc1 es una enzima que puede metilar las histonas. Aun así, la función de Whsc1 en la salida de pluripotencia y la diferenciación del mesendodermo es independiente de su dominio catalítico, y por tanto de esta función.
- Whsc1 se une a los elementos reguladores de los genes «maestros» de linaje Gata4, T (Brachyury), Gata6 y Foxa2 y los activa, dando lugar a una especificación de células germinales. Esto lo hace junto con la proteína Brd4.
Los autores concluyen que Whsc1 vincula el silenciamiento de la red reguladora de pluripotencia con la activación de los linajes del mesendodermo y, por lo tanto, juega un papel clave en esta importante transición del embrión.
El laboratorio de Thomas Graf ha encontrado que el factor relacionado con la cromatina Whsc1 juega un papel clave en la diferenciación del embrión; vincula la salida de pluripotencia con la especificación del linaje del mesodermo.
«Nuestro descubrimiento anula el antiguo concepto de que las células pluripotentes deben olvidar primero quiénes son antes de poder aprender nuevas reglas que les permitan cambiar de identidad. Por qué y cómo Whsc1 sólo establece una conexión con dos de las tres capas germinales es una pregunta interesante para el futuro», dice Thomas Graf, líder de este estudio, realizado en colaboración con la Universidad de Harvard, el Instituto Whitehead para la Investigación Biomédica y el MIT en Cambridge, EEUU.
En este vídeo (en inglés) el jefe de grupo, Thomas Graf, nos explica este descubrimiento.
Tian V. Tian et al. Whsc1 links pluripotency exit with mesendoderm specification. Nat Cell Biol. 2019 Jul;21(7):824-834. doi: 10.1038/s41556-019-0342-1. Epub 2019 Jun 24.





De esto podemos aprender más 👍🏻
Interesante artículo, muchas gracias por compartir