El cambio climático está favoreciendo las condiciones para la reproducción y diseminación de enfermedades infecciosas típicas de climas tropicales, como es el caso de los virus Zika, Chikungunya o Dengue, que se transmiten por la picadura de un mosquito. Estos virus son de especial interés ya que pueden atravesar la barrera hematoencefálica (BHE) y penetrar en el cerebro, donde pueden causar daños irreversibles. Además el Zika, si infecta durante el embarazo, es capaz de penetrar también la barrera placentaria (BP), produciendo daños en el cerebro del bebé, su nacimiento prematuro o incluso el aborto.
El proyecto NOVIRUSES2BRAIN, que ha concedido a la UPF 1,6 M€ del programa europeo FETOPEN-Horizon 2020, tiene como objetivo encontrar un fármaco que sea capaz de atravesar tanto la BHE como la BP para poder atacar a los virus que llegan al cerebro o al feto. Se puso en marcha hace cuatro años y cuenta con personal investigador del Departamento de Medicina y Ciencias de la Vida de la Universidad Pompeu Fabra (MELIS-UPF), del Instituto de Medicina Molecular de Lisboa y de Synovo GmbH en Tubinga.
Hablamos con David Andreu y Toni Todorovski investigadores del MELIS-UPF para conocer mejor el proyecto.
¿Por qué es importante encontrar este tipo de antiviral?
En los últimos 10 años, las epidemias víricas como la del SARS-CoV-2, la gripe, o la del Zika que azotó Sudamérica entre 2015-2016, son cada vez más comunes. Y aunque la investigación con antivirales es intensa, desde 1963 solo se han aprobado un total de 90 fármacos para 9 virus humanos, unos datos sorprendentes cuando se comparan con los que existen para tratar la diabetes o la tensión arterial, por ejemplo.
Más grave aún, el arsenal de tratamientos para luchar contra los virus que afectan al cerebro es todavía más limitado. Una de las razones es que, aunque hay antivirales que funcionan relativamente bien in vitro, son incapaces de cruzar la BHE; algo comprensible, ya que para eso está esta barrera, para no dejar que nada entre al cerebro. El problema es que algunos virus lo consiguen… pero los antivirales no, y esto los hace ineficaces.
¿Entonces, el objetivo principal del proyecto es conseguir atravesar la barrera del cerebro?
En efecto; con este proyecto no pretendemos descubrir un nuevo fármaco antiviral, esos ya existen. Lo que buscamos es encontrar una nueva manera de administrar antivirales para que lleguen al virus y puedan atacarlo eficazmente. El problema que tenemos pues es llegar hasta un virus que ha atravesado estas barreras del cerebro o la placenta. Una vez sepamos llegar hasta él, tenemos fármacos para eliminarlo.
Podríamos decir que diseñamos contrabandistas que, con una mochila cargada de antivirales ya existentes, sean capaces de cruzar por sitios donde es casi imposible cruzar. Para que una vez en el otro lado, el paquete (el antivirus), despliegue su potencial y actúe allí donde haga falta.
“Nuestro objetivo es explorar los virus que no pueden atravesar ni la BHE ni la BP y proponer soluciones que dirijan los fármacos hasta allí donde se encuentren estos virus. Aunque es un objetivo ambicioso al que nadie se ha enfrentado antes nuestros primeros resultados son prometedores”
Para alcanzar el objetivo hemos definido tres fases del proyecto:
- Desarrollo de conjugados vector + fármaco (contrabandista + mochila) de alto rendimiento, la principal área de trabajo en MELIS-UPF.
- Ensayos in vitro para comprobar la penetración del conjugado tanto a través de la BHE como de la BP, y la eficacia del componente antiviral en estos casos.
- Ensayos in vivo de los conjugados con mayor potencial antiviral en la fase anterior. Es la fase con mayor actividad actualmente, y la más compleja ya que, aunque haya buenos resultados in vitro, al pasar a in vivo suele haber muchas sorpresas.
¿Y cómo conseguís que este nuevo tratamiento atraviese la barrera?
El tratamiento consiste en un conjugado, es decir la unión de un fármaco con propiedades antivirales y un vector encargado de transportarlo.
- Los fármacos, en nuestro caso, son porfirinas, antivirales de amplio espectro pero incapaces de atravesar la BHE o la BP.
- El vehículo o vector, son péptidos penetradores, cell penetrating peptides (CPP), que sí son capaces de atravesar tanto la BHE como la BP de manera efectiva, pero que por sí solos no tienen propiedades antivirales.
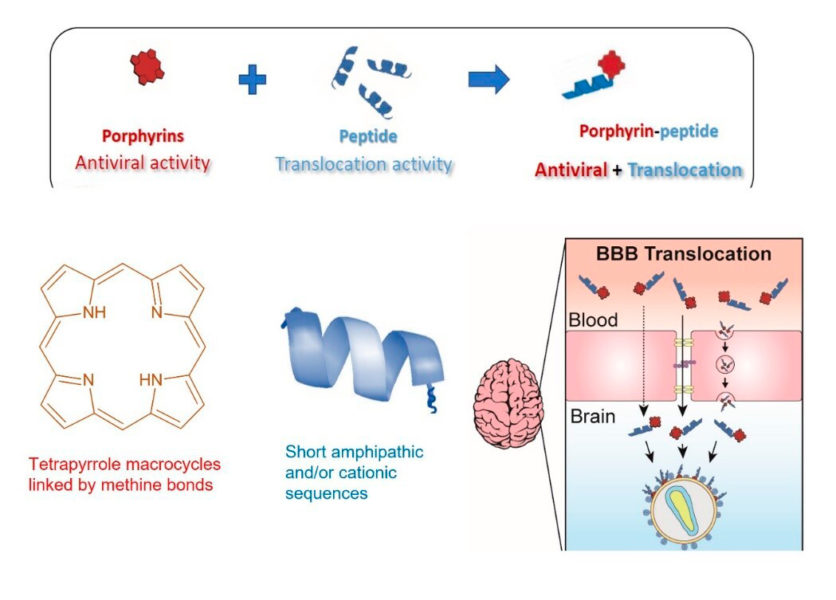
Nuestro trabajo ha consistido en enlazar estas dos moléculas para poder administrar el fármaco en cantidades suficientes allí donde se encuentra el virus. ¡Algo que parece sencillo, pero en lo que llevamos trabajando unos tres años…!
¿Por qué es tan difícil?
Combinando 6 péptidos, 5 tipos de porfirinas y un conector, hemos diseñado y producido 24 conjugados diferentes. Es un diseño en que hemos tenido en cuenta la posición de unión de la porfirina en la estructura del CPP, la distancia entre ambos elementos, etc. para conseguir una molécula óptima con buena tasa de translocación y a la vez capaz de mantener y desplegar las propiedades antivirales. Otro aspecto esencial, y relativamente imprevisible, es la toxicidad, que puede descarrilar algunos candidatos…
¿Qué resultados habéis obtenido? ¿Cuáles son los próximos pasos?
Nuestro proyecto es de ciencia básica: diseñar conjugados eficaces tanto in vitro como en un modelo in vivo, de ratón, que permitan plantear nuevas estrategias terapéuticas contra virus que afectan tanto al cerebro como al feto. Los estudios in vivo actualmente en marcha indican que tenemos un conjugado ganador y un finalista. Concretamente, los resultados están siendo muy buenos frente al virus Zika; pero, además, algunos conjugados son multivalentes, con efecto sobre otros virus como VIH o SARS-CoV-2. En base a los resultados contra Zika hemos patentado ya varias de estas nuevas moléculas diseñadas en el laboratorio y a partir de ahí podrán entrar en juego empresas farmacéuticas que desarrollen estas moléculas como fármacos, aunque aún estamos lejos de un antiviral multivalente.







