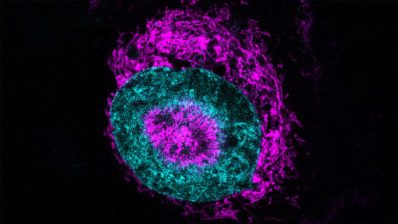
A l’igual que en d’altres malalties neurodegeneratives, els agregats proteïcs són presents al cervell i medul·la espinal de la immensa majoria de pacients amb esclerosi lateral amiotròfica (ELA). Però no està clar si aquests agregats són els causants reals de les malalties.
Agregació proteïca: causa o conseqüència?
Per tal d’esbrinar-ho, personal investigador del Centre de Regulació Genòmica (CRG) i l’Institut de Bioenginyeria de Catalunya (IBEC) han utilitzat una tècnica anomenada mutagènesi. Van agafar TDP-43, una proteïna que s’acumula a les motoneurones de pràcticament tots els pacients amb ELA, i van crear al voltant de 50.000 versions d’aquesta, cadascuna amb una mutació diferent. Posteriorment, van introduïr cada versió en cèl·lules de llevat i van quantificar-ne la toxicitat.
Resultats sorprenents
Sorprenentment, les proteïnes mutades que causaven agregació van resultar ser les menys tòxiques en llevats i, en canvi, les versions més tòxiques es trobaven en estat líquid. Segons Ben Lehner, líder de l’estudi, això és exactament el contrari al que esperaven trobar segons l’actual coneixement sobre aquestes malalties. “Sembla que l’agregació protegeix les cèl·lules, enlloc de malmetre-les”, coincideix Benedetta Bolognesi, primera co-autora de l’article – juntament amb André Faure – i, actualment, líder de grup junior a l’IBEC.
“Cal tenir en compte que l‘estudi s’ha dut a terme en llevats, que és un sistema model – no sabem si en humans hi ha altres aspectes en joc… Però el que aquest experiment ens demostra és que l’agregat en sí mateix, en estat sòlid, no mata a les cèl·lules eucariotes. I això és important, perquè tots els articles publicats sobre malalties neurodegeneratives, com l’Alzheimer o el Pàrkinson, comencen dient “els agregats insolubles o les plaques són un dels distintius de la malaltia”; i això és cert, però no significa que siguin la causa de la malaltia”, afirma la investigadora italiana.
“És possible que les formes perjudicials siguin intermediaris en el procés d’agregació, però també es podrien estar formant independentment dels agregats; podrien no estar relacionats. No ho hem mesurat”, alerten els autors.
Els autors van crear >50.000 formes mutants de TDP-43, la proteïna que s’acumula als cervells dels pacients amb Esclerosi Lateral Amiotròfica (ELA). Han vist que els agregats proteïcs com a tals no maten a les cèl·lules de llevat.
Bolognesi comprovarà ara si això (que les formes líquides són perjudicials i els agregats no) és cert en cèl·lules de mamífer. Si es confirma, estariem davant d’un punt d’inflexió en l’estudi de les malalties neurodegeneratives com l’ELA o l’Alzheimer, el tractament de les quals ha estat centrat en evitar aquests agregats proteïcs, sense èxit.
“El que m’agrada d’aquest article, i de la metodologia emprada, és que gràcies a que vam analitzar totes les mutacions possibles podem veure alguns patrons que no veuriem a l’analitzar una sola mutació”, afegeix Bolognesi.
Les mutacions genètiques poden indicar l’estructura de les proteïnes
La metodologia emprada, l’escaneig profund de mutacions (deep mutagenesis scanning), implica crear milers de versions mutades de la mateixa proteïna i analitzar-les després. El mètode, publicat recentment pel laboratori de Lehner, ha demostrat en l’estudi del TDP-43, ser capaç d’oferir pistes sobre l’estructura de les proteïnes i com aquesta afecta a les cèl·lules.
Desxifrar l’estructura 3D de les proteïnes es fa, normalment, per diversos mètodes com la cristal·lografia de raigs X, l’espectroscòpia de ressonància magnètica nuclear (RMN) o la criomicroscòpia electrònica. Totes aquestes metodologies, però, tenen limitacions i solen ser cares. La predicció computacional a partir de seqüències d’aminoàcids no és tan cara, però no sempre és precisa.
El personal investigador del CRG va implementar una aproximació més barata i simple: prendre una proteïna, mutar cadascun dels seus aminoàcids i, després, analitzar com cada mutació afecta el creixement de les cèl·lules que contenen la mutació. Trobant relacions entre mutacions els efectes de les quals combinnen de maneres inesperades, i assumint que segurament aquestes mutacions seran colindants en la proteïna plegada, els científics poden inferir l’estructura en 3D de la proteïna.
“Tot i que l’escaneig profund de mutacions podria ser considerat un mètode experimental molt establert, existeix una gran necessitat d’utilitzar eines computacionals fàcils d’emprar per tal d’analitzar i interpretar els resultats obtinguts, tal i com vam fer en aquest article. Aquest és el motiu pel qual estem desenvolupant DiMSum: un software gratuït per processar resultats obtinguts a partir de l’escaneig profund de mutacions”, afegeix André Faure, qui va dirigir l’anàlisi de dades en l’article sobre el TDP-43.
Benedetta Bolognesi, Andre J. Faure, Mireia Seuma, Jörn M. Schmiedel, Gian Gaetano Tartaglia & Ben Lehner. The mutational landscape of a prion-like domain. Nature Communications volume 10, Article number: 4162 (2019)
Jörn M. Schmiedel & Ben Lehner. Determining protein structures using deep mutagenesis. Nature Genetics volume 51, pages1177–1186 (2019)