El Grup de Recerca en Virologia Molecular del Departament de Medicina i Ciències de la Vida, Universitat Pompeu Fabra (MELIS-UPF), dirigit per Juana Diez, i el grup d’Epitranscriptoma i dinàmica d’ARN del Centre de Regulació Genòmica (CRG), dirigit per Eva M. Novoa han liderat un estudi sobre com els virus reprogramen la maquinària cel·lular hoste en el seu benefici per així reproduir-se de forma més eficient.
En concret, els equips científics han observat que la infecció viral indueix una reprogramació de les modificacions dels ARNt cel·lulars per a afavorir la traducció dels codons virals. Així, maximitzen l’expressió de les proteïnes i, per tant, la infecció viral.
La paradoxa de l’eficient traducció viral
Els virus depenen completament de la maquinària de traducció de la cèl·lula hoste. Per a expressar les proteïnes virals a partir del seu material genètic, els virus necessiten els ARNt (ARN de transferència) de la cèl·lula. Aquests detecten els codons de l’ARN viral que determinen un aminoàcid o un altre.
El codi genètic que estableix a quin aminoàcid correspon cada codó és redundant, cosa que permet que un aminoàcid estigui codificat per més d’un codó. La freqüència d’aquests codons sinònims no és aleatòria, sinó que està esbiaixada i és específica de cada organisme. Com que la concentració dels ARNt a cada organisme està adaptada a aquesta freqüència, els codons subòptims alenteixen la traducció perquè els ARNt corresponents són poc abundants en comparació dels ARNt que reconeixen els codons òptims.
La dependència viral dels ARNt cel·lulars és especialment crítica per als virus RNA de cadena positiva (RNA+), el primer pas dels quals en el cicle d’infecció és precisament la traducció de l’RNA viral. El grup de virus RNA+ inclou molts virus patògens humans, incloent virus nous i emergents com ara el SARS CoV-2 o els virus transmesos per mosquits com el dengue, el zika o el chikungunya.
Tots aquests virus expressen les seves proteïnes a nivells altíssims. Tot i això, els genomes d’aquests virus estan enriquits en codons subòptims i, per tant, s’haurien de traduir ineficientment. Per resoldre aquesta paradoxa els autors van fer servir com a model d’estudi el virus chikungunya pel seu alt nivell de replicació.
El secret és a l’epitranscriptoma
El treball del MELIS-UPF i el CRG, que també ha comptat amb la col·laboració d’investigadores de la Universitat de Tartu, ha observat que la infecció pel virus del chikungunya indueix un estrès cel·lular que porta a un augment de la producció de l’enzim de modificació de l’ARNt KIAA1456. Això comporta canvis en l’epitranscriptoma (el conjunt de modificacions químiques que pateix l’ARN) que afavoreixen el reconeixement per part dels ARNt cel·lulars de codons subòptims, presents en proteïnes cel·lulars de resposta a estrès i també al virus. Així, aquests codons passen a ser, a nivell pràctic, òptims. Per tant, el genoma del virus chikungunya ha evolucionat perquè la composició dels seus codons sigui òptima en les condicions d’infecció de la cèl·lula hoste.
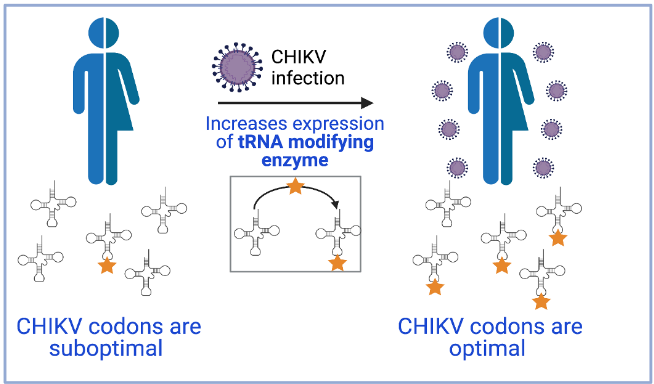
“Encara que l’estudi s’ha centrat en el virus del chikungunya, hem confirmat que altres virus utilitzen una estratègia similar per afavorir l’expressió de les seves proteïnes, per això proposem que la modificació dels ARNt induïts per la infecció viral és un mecanisme general seguit per molts virus”
Juana Díez, cap del grup del MELIS-UPF i investigadora principal de l’estudi
Els experiments s’han realitzat amb línies cel·lulars ja establertes de cèl·lules humanes del fetge, cèl·lules renals embrionàries i fibroblasts de ronyó. El descobriment posa els enzims de modificació de l’ARNt al punt de mira a l’hora d’estudiar altres virus i noves dianes terapèutiques per al desenvolupament d’antivirals de gran espectre.
Jungfleisch J et al. CHIKV infection reprograms codon optimality to favor viral RNA translation by altering the tRNA epitranscriptome. Nature Communications. August, 2022. DOI: 10.1038/s41467-022-31835-x.