Mitsuhiro Matsuda, dirigido por Miki Ebisuya en el Laboratorio Europeo de Biología Molecular – Barcelona (EMBL Barcelona), ha colaborado con compañeros y compañeras de varias instituciones japonesas para recapitular in vitro el mecanismo genético subyacente a las estructuras periódicas de nuestra columna vertebral.
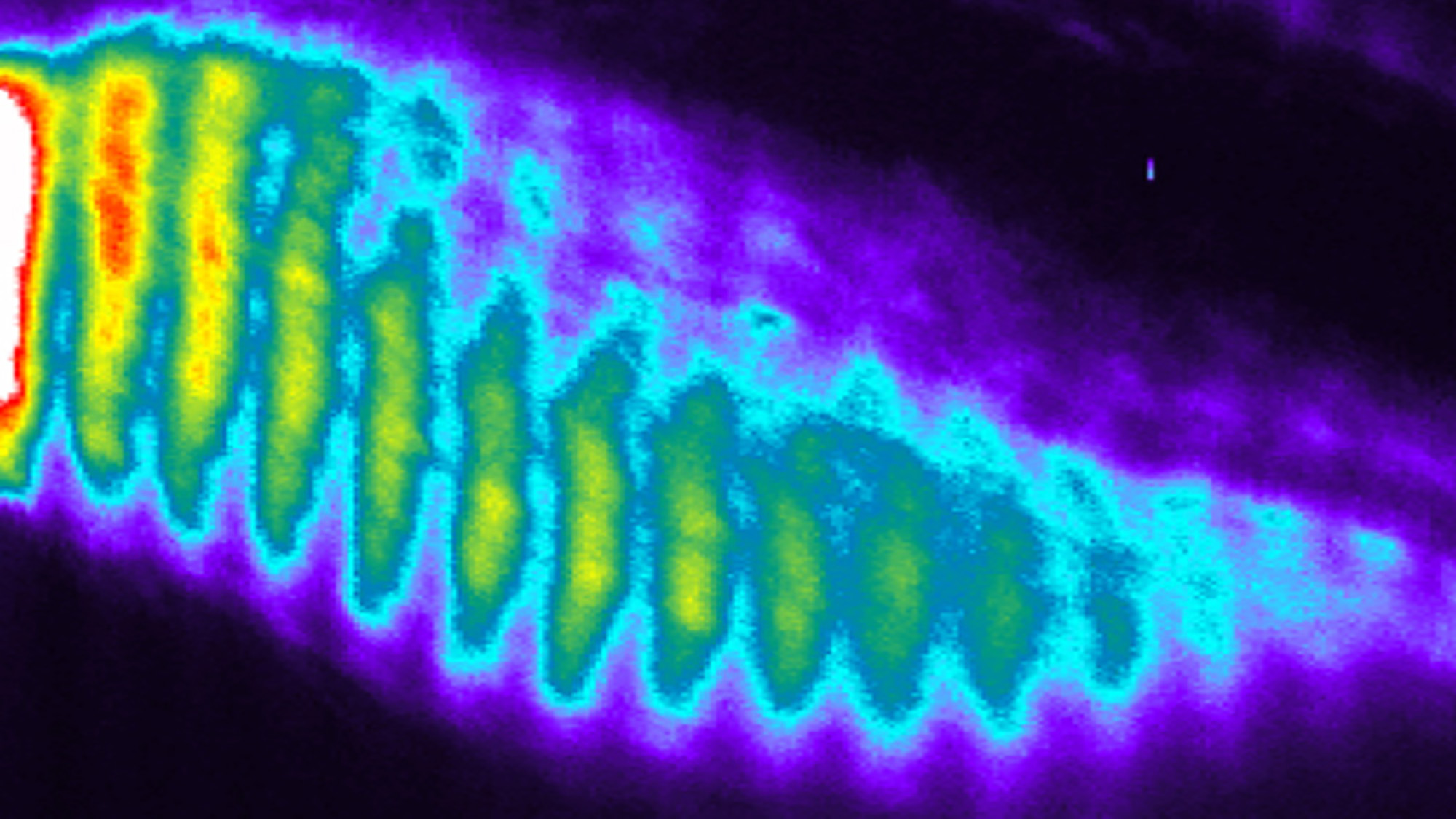
La expresión de este grupo de genes, conocidos como «reloj de segmentación«, oscila durante el desarrollo embrionario, cuando la actividad genética aumenta y disminuye en un patrón regular en el tiempo (ver vídeo abajo). Para cada oscilación, se forma un nuevo somita, los predecesores de las vértebras y costillas. Errores en el reloj de segmentación pueden provocar trastornos hereditarios de las vértebras, tales como la disostosis espondilocostal (SCD).
Los y las investigadoras crearon líneas celulares a las que les faltaban uno de los genes conocidos por causar SCD – HES7, DLL3 o LFNG – y observaron que las oscilaciones genéticas no tenían lugar, o no se coordinaban correctamente a lo largo del tejido para formar las ondas viajeras habituales de la actividad genética. Luego verificaron que lo mismo sucedía con células de pacientes reales (con DLL3 mutado), y finalmente usaron la herramienta de edición genética CRISPR-Cas9 para corregir la mutación del paciente, demostrando que esta mutación era efectivamente la responsable de la asincronía del reloj de segmentación.
Podéis leer más sobre este estudio en la página web de EMBL.
Matsuda M et al. Recapitulating the human segmentation clock with pluripotent stem cells. Nature, published 1 April 2020. DOI: 10.1038/s41586-020-2144-9.