El canvi climàtic està afavorint les condicions per a la reproducció i disseminació de malalties infeccioses típiques de climes tropicals, com és el cas de les causades pels virus Zika, Chikungunya o Dengue, que es transmeten per la picada d’un mosquit. Aquests virus són d’especial interès ja que poden travessar la barrera hematoencefàlica (BHE) i penetrar al cervell, on poden causar danys irreversibles. A més, en el cas del Zika, si aquest infecta durant l’embaràs, és capaç de penetrar també la barrera placentària (BP), produint danys al cervell del bebè, el seu naixement prematur o fins i tot l’avortament.
El projecte NOVIRUSES2BRAIN, que ha concedit a la UPF 1,6 M€ del programa europeu FETOPEN-Horizon 2020, té com a objectiu trobar un fàrmac que sigui capaç de travessar tant la BHE com la BP per a poder atacar els virus que arriben al cervell o al fetus. Es va posar en marxa fa gairebé quatre anys i compta amb personal investigador del Departament de Medicina i Ciències de la Vida de la Universitat Pompeu Fabra (MELIS-UPF), de l’Institut de Medicina Molecular de Lisboa i del Synovo GmbH a Tübingen.
Parlem amb en David Andreu i en Toni Todorovski, investigadors del MELIS-UPF, per a conèixer millor el projecte.
Per què és important generar fàrmacs contra aquests virus?
Els últims 10 anys, les pandèmies víriques com la del SARS-CoV-2, la grip o la del Zika que va colpejar Sudamèrica entre 2015-2016, són cada cop més comunes. I malgrat que la recerca amb antivirals és intensa, des de 1963 només s’han aprovat un total de 90 fàrmacs per a 9 virus humans, unes dades sorprenents quan es comparen amb els existents per a tractar la diabetis o la tensió arterial, per exemple.
Més greu encara, l’arsenal de tractaments per a lluitar contra els virus que afecten el cervell és encara més limitat. Una de les raons és que, malgrat que hi ha antivirals que funcionen relativament bé in vitro, són incapaços de travessar la BHE; cosa que té prou sentit, ja que per a això està la barrera, per a no deixar que res entri al cervell. El problema és que alguns virus sí que ho aconsegueixen… però els antivirals no, i això els fa ineficaços.
Llavors, l’objectiu principal del projecte és aconseguir travessar la barrera del cervell?
En efecte; amb aquest projecte no pretenem descobrir un nou fàrmac antiviral, aquests ja existeixen. El que busquem és trobar una nova manera d’administrar antivirals per a què arribin al virus i puguin atacar-lo de manera eficaç. El problema que tenim, doncs, és arribar fins a un virus que ha travessat aquestes barreres del cervell o la placenta. Un cop sapiguem arribar fins a ell, tenim fàrmacs per a eliminar-lo.
Podríem dir que dissenyem “contrabandistes” que, amb una motxilla carregada d’antivirals ja existents, siguin capaços de creuar per llocs on és gairebé impossible creuar. D’aquesta manera, un cop a l’altre costat, el paquet (l’antivirus) pot desplegar el seu potencial i actuar allà on calgui.
“El nostre objectiu és explorar els virus que poden travessar la BHE i la BP i proposar solucions que dirigeixin els fàrmacs cap allà on es trobin aquests virus. Malgrat que és un objectiu ambiciós al qual ningú s’hi ha enfrontat amb anterioritat, els nostres primers resultats són prometedors”
Per a assolir l’objectiu hem definit tres fases del projecte:
- Desenvolupament de conjugats vectors + fàrmac (contrabandista + motxilla) d’alt rendiment, la principal àrea de treball al MELIS-UPF.
- Assajos in vitro per a comprovar la penetració del conjugat a través de la BHE i la BP, i l’eficàcia del component antiviral en aquests casos.
- Assajos in vivo dels conjugats amb major potencial antiviral a la fase anterior. És la fase amb major activitat actualment, i la més complexa ja que, tot i que els resultats in vitro puguin ser bons, en passar a in vivo solem trobar-nos moltes sorpreses.
I com aconseguiu que aquest nou tractament travessi la barrera?
El tractament consisteix a desenvolupar un conjugat, és a dir, la unió d’un fàrmac amb propietats antivirals i d’un vector encarregat de transportar-lo.
- Els fàrmacs, en el nostre cas, són porfirines, antivirals d’ampli espectre, però incapaces de travessar la BHE o la BP.
- El vehicle o vector, són pèptids penetrants, cell penetrating peptides (CPP) en anglès, que sí són capaços de travessar tant la BHE com la BP de manera efectiva, però que per sí mateixos no tenen propietats antivirals.
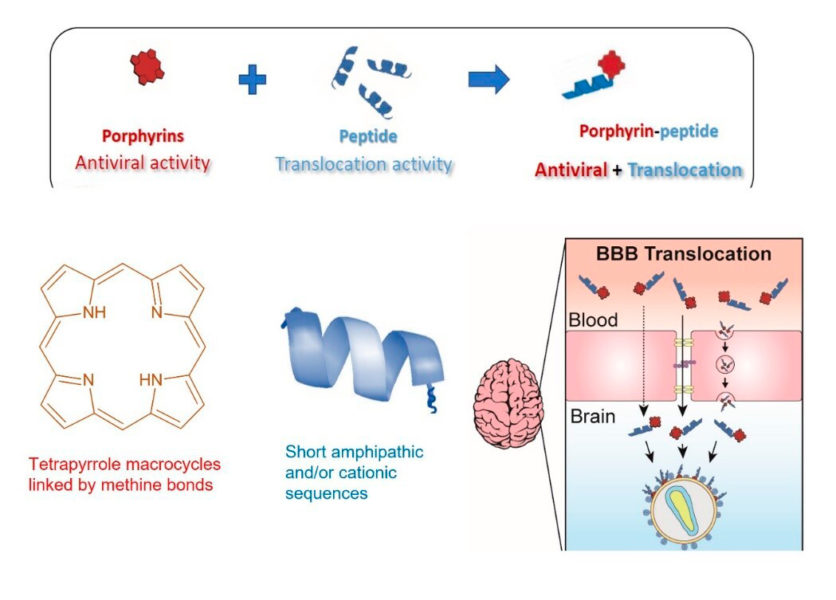
La nostra feina a consistit a enllaçar aquestes dues molècules per a poder administrar el fàrmac en quantitats suficients allà on es troba el virus. Cosa que sembla senzilla, però hi portem treballant uns tres anys…!
Per què és tan difícil?
Combinant 6 pèptids, 5 tipus de porfirines i un connector, hem dissenyat i produït 24 conjugats diferents. És un disseny on hem tingut en compte la posició d’unió de la porfirina a l’estructura del CCP, la distància entre els dos elements, etc. per a aconseguir una molècula òptima amb bona taxa de translocació i, alhora, capaç de mantenir i desplegar les propietats antivirals. Un altre aspecte essencial, i relativament imprevisible, és la toxicitat, que pot descarrilar alguns candidats…
Quins resultats heu obtingut? Quins són els pròxims passos?
El nostre projecte és de ciència bàsica: dissenyar conjugats eficaços tant in vitro com en un model in vivo de ratolí que permetin plantejar noves estratègies terapèutiques contra virus que afecten tant al cervell com al fetus. Els estudis in vivo actualment en marxa, indiquen que tenim un conjugat guanyador i un de finalista. Concretament, els resultats són molt bons davant el Zika; però, a més, alguns conjugats són multivalents, amb efecte sobre altres virus com el VIH o SARS-CoV-2. En base als resultats contra el Zika hem patentat ja algunes d’aquestes noves molècules dissenyades al laboratori i a partir d’aquí, podran entrar en joc empreses farmacèutiques que desenvolupen aquestes molècules com a fàrmacs. Però encara són lluny de tenir un antiviral multivalent.







