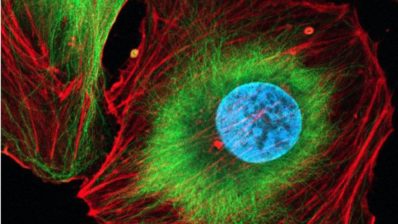
Hay más de lo que parece a primera vista en el Parque de Investigación Biomédica de Barcelona (PRBB)– en sentido figurado y literal. Fuera de la vista, en la planta -1 del edificio, se encuentra no tan sólo uno de los más complejos y robotizados animalarios en Europa, sino también dos instalaciones de imagen de última generación: la instalación de imagen de mesoscopia (MIF) del Laboratorio Europeo de Biología Molecular – Barcelona (EMBL Barcelona) y la Unidad de Microscopia Óptica Avanzada (ALMU) del Centro de Regulación Genómica (CRG), situadas en el mismo espacio. «Durante los últimos 6 años, hemos ofrecido servicios complementarios al ALMU; ellos ofrecen microscopía confocal y a escala de superresolución. Nosotros ofrecemos mesoscopía», afirma Gopi Shah, Gerente de Iniciativas Estratégicas de Imagen del MIF, EMBL Barcelona.
Mesoscopía: el punto intermedio
La microscopía se ocupa de cosas muy pequeñas: muestras de tamaño nano a micro, como secciones de tejidos, células individuales, estructuras subcelulares, orgánulos, etc. Al otro extremo están los rayos X, las resonancias magnéticas, las tomografías computadas y otras tecnologías que asociamos más a menudo con los hospitales y que son útiles para mirar al nivel del paciente humano. La mesoscopía representa la escala intermedia y añade volumen.
Las muestras habituales que se observan con sistemas de mesoscopía son embriones enteros de organismos modelo (embriones de mosca, embriones de peces, embriones de ratón) u órganos enteros de organismos modelo adultos, como el cerebro, los pulmones, los riñones, la melsa, los ovarios, etc.
El tipo de tamaños que se pueden ver con mesoscopía van desde unos pocos centenares de micras hasta unos pocos centímetros, con algunas excepciones. «Hemos podido visualizar el crecimiento y el desarrollo de organoides vivos y otros modelos in vitro que se han desarrollado en los últimos años. Tienen un tamaño de unos cuantos centenares de micras, por lo que son más pequeños de lo habitual para la mesoscopía, pero es difícil obervarlos con otros microscopios (confocales, de superresolución) ya que son muestras 3D y densamente empaquetadas», explica Gopi. Y añade: «Por ello nuestros sistemas son útiles para estos organoides, ya que nos permiten ver muestras desde múltiples direcciones y reconstruir un volumen 3D completo. También conseguimos observar con algunos de nuestros sistemas, muestras de 20-50 micras que nos traen investigadores del Instituto de Ciencias del Mar (ICM – CSIC)«.
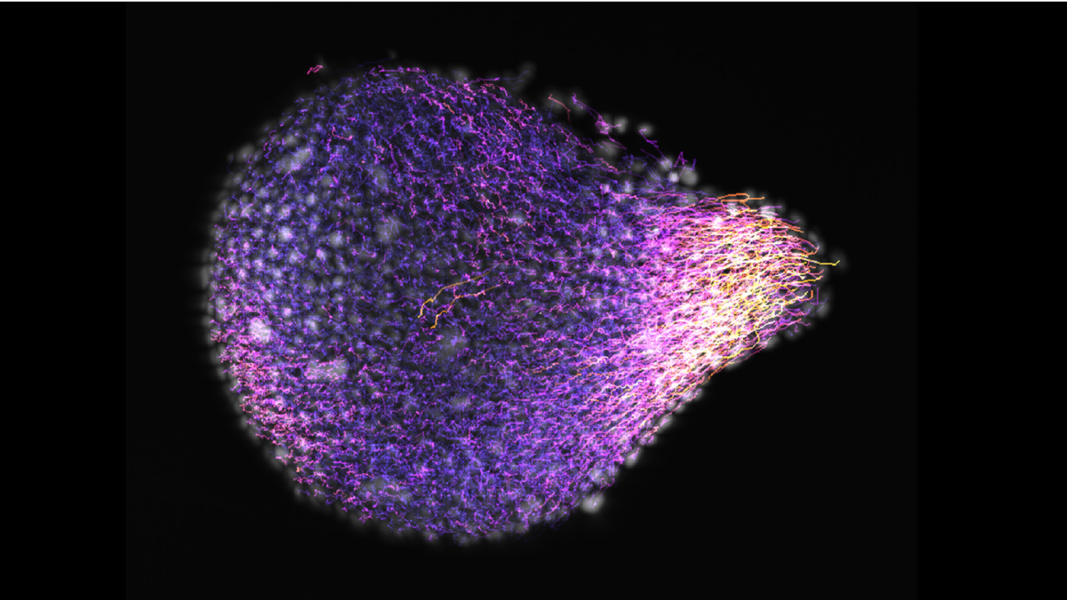
El MIF está abierto a todo el mundo, ya que recibe financiación básica del Laboratorio Europeo de Biología Molecular, la mayor infraestructura europea de Ciencias de la Vida. «Estamos encantados de trabajar con usuarios e instituciones muy diversos, desde colegas del EMBL hasta nuestros vecinos del Parque de Investigación Biomédica de Barcelona (PRBB), laboratorios, hospitales o socios de la industria en Barcelona y más allá. Nuestro principal objetivo es dar un servicio de vanguardia a la comunidad científica», afirma la gerente del MIF.
Nuestro principal objetivo es dar un servicio de vanguardia a la comunidad científica, venga de donde venga.
Gopi Shah, Gerente de Iniciativas Estratégicas de Imagen, MIF, EMBL Barcelona
En cuanto al coste, añade: «Hasta ahora, no hemos cobrado por utilizar la instalación. Cada nuevo sistema necesita hacer muchas pruebas hasta estar listo, y los usuarios nos han ayudado. Por lo tanto, actualmente estamos gestionando la instalación con un enfoque colaborativo y en el futuro nuestros servicios podrán ser a precios asequibles. Estamos comprometidos a construir colaboraciones y ofrecer un servicio de imagen de vanguardia a tantos laboratorios como sea posible».
Diferentes microscopios y diferentes técnicas
La microscopía de fluorescencia de lámina de luz (LSFM, también llamada microscopía de iluminación plana selectiva o SPIM) es el principal tipo de imagen que se hace en la instalación. Disponen de 2 equipos caseros y 3 comerciales, cada uno con aplicaciones diferentes. Los caseros se pueden personalizar para cosas que no se pueden hacer con los comerciales. Observan muestras grandes, como un embrión de ratón entero o incluso el cerebro de un ratón adulto, con una resolución de una sola célula. «También utilizamos estos sistemas para obtener imágenes de organoides vivos: puedes hacer imágenes durante días y los organoides están cómodos allí!», explica Gopi.
La tomografía de proyección óptica (OPT), otra de las técnicas que ofrecen, utiliza una fuente de luz y una cámara, poniendo la muestra en medio. Funciona haciendo girar la muestra 1 grado cada vez y haciendo una foto. Así, se acaba con 360 imágenes (360°) y se puede reconstruir el objeto 3D, de la misma manera que un sistema de rayos X en una clínica permite a los médicos hacer una reconstrucción 3D de tus huesos. Estos son útiles para muestras más grandes, y la instalación posee dos máquinas OPT, una comercial y otra casera.
Un tercer tipo de tecnología que tienen a la instalación es la holotomografía: permite obtener imágenes en directo de cultivos celulares en una placa y láminas planas de células que no necesitan etiquetas (ni colorantes ni etiquetas fluorescentes), ya que utiliza el contraste inherente que proviene del hecho de que cada compartimento de una célula tiene un índice de refracción diferente. Así se pueden ver los orgánulos dentro de las células. La única limitación es que sólo puede capturar una profundidad de 30 micras.
Todos estos sistemas de imagen permiten diferentes maneras de visualizar las muestras, ya sean vivas o tratadas.
«Podemos hacer aclaramiento de tejidos, que es una técnica para profundizar en una muestra; se aplican productos químicos para que se vuelva transparente y uniforme en su índice de refracción», explica Gopi, que añade que esto es útil para ver un órgano de ratón entero o incluso un ratón adulto entero. «Se puede diseccionar un órgano, hacer el etiquetado, hacer el aclaramiento de tejidos con los reactivos químicos y mirarlo con microscopía de lámina de luz u OPT». La holotomografía es la única que no se puede utilizar para muestras ‘aclaradas’.
Además de sus microscopios y técnicas especializadas, disponen de algunos equipos más habituales, como un microscopio de epifluorescencia para ejecutar un time-lapse, o para comprobar si el etiquetado de las muestras ha funcionado correctamente; una campana de cultivo de tejidos por si se necesita alguna pequeña manipulación; y una zona de laboratorio donde los usuarios pueden preparar sus muestras si es necesario.
Un proceso paso a paso
Normalmente, cuando un usuario o usuaria está interesada en utilizar la instalación, se sigue un proceso de 3 pasos:
- Reunión/consulta donde los investigadores explican qué quieren conseguir. El personal de la instalación les muestra lo que tienen y deciden qué es posible y qué es lo más adecuado para la tarea.
- Los usuarios reciben formación (2-3 sesiones) y luego pueden registrarse, reservar y utilizar los instrumentos. También se les asesora sobre la preparación de muestras: cómo mantenerlas vivas, cómo hacer el montaje de muestras y el aclaramiento de tejidos, etc.
- Procesamiento de imágenes y visualización y análisis de datos: el MIF cuenta con una persona dedicada al procesamiento de imágenes para ayudar a los usuarios y usuárias a manejar los datos; también puede escribir códigos personalizados para ayudar en el análisis de imágenes.
La unidad genera toneladas de imágenes. «El light-sheet es muy rápido: puede grabar el latido del corazón de un pez cebra, una estructura 3D que late 2 veces por segundo», dice Gopi. Según ella, si se utilizan todos los instrumentos de la instalación, son varios terabytes de datos al día. Es por ello que ofrecen un espacio de almacenamiento de datos temporal donde los usuarios pueden guardar los datos para el procesamiento y el análisis posterior.
Un equipo experto
El MIF es un equipo interdisciplinario e internacional de 5 personas, con formación en biología, ingeniería y física.
«Tenemos 2 ingenieros ópticos, 2 biólogos y un analista de imágenes que juntos permiten acompañar durante todos los pasos de un experimento de imagen. Pero todo el mundo, sea cual sea sus estudios iniciales, se ha especializado en imágenes», explica Gopi, que tiene experiencia en imágenes de muestras en vivo.

Montserrat Coll Lladó es la experta en el aclaramiento de tejidos. También tienen dos ingenieros ópticos que construyen los microscopios. Jim Swoger, que también es el jefe de la instalación, y Spyridon Bakas, que actualmente está trabajando en el desarrollo de un nuevo sistema de sobremesa y en personalizar los sistemas comerciales. Por ejemplo, si un experimento necesita un nuevo soporte para las muestras, o alguien necesita alguna herramienta física, los hace en el microfablab, situado en la planta -2 del PRBB. Para los equipos caseros, a veces las piezas son comerciales y a veces diseñadas específicamente en un taller o impresas en 3D. Obviamente necesitan condiciones especializadas para desarrollar estos sistemas, y tienen grandes mesas antivibraciones en la instalación para su desarrollo.
Nicola Gritti es un experto en el manejo, procesamiento y análisis de datos de imágenes. Ayuda a los y las usuarias con la formación y la personalización de los procesos de procesamiento de imágenes. En conjunto, el equipo ofrece soporte de principio a fin a los usuarios de la instalación.
Microscopía de expansión
El equipo ha estado experimentando últimamente para intentar ver cosas más pequeñas. Hay dos maneras principales de conseguirlo:
- La manera óptica. Normalmente no se pueden ver dos objetos que estén a menos de 200 nm, pero con técnicas de microscopía de superresolución se puede bajar hasta 20 nm. Esta microscopía de superresolución está disponible en la unidad ALMU del CRG, que comparte espacio con el MIF.
- Expandiendo las muestras isotrópicamente. Esto quiere decir separar todas las estructuras y moléculas de una muestra, pero de manera que la relación entre ellas sea la misma. Esto se puede hacer poniendo la muestra en un polímero (un tipo de gel) que se expande en presencia de agua. De esta manera se puede expandir algo de 4 a 10 veces en una dirección. «Montserrat Coll Lladó y su estudiante de prácticas de la UPF, Laura Campamé, lo hicieron con un embrión de ratón de 12 días; ¡fue como utilizar un zoom muy potente!», remarca Gopi.
«Recientemente hemos estado emocionados probando nuevas técnicas, incluida la microscopía de expansión. ¡Hay tantas posibilidades! Estamos encantados de hablar con cualquier persona interesada en utilizar nuestras instalaciones y ver qué puede hacer la mesoscopía por su investigación; ¡queremos hacer proyectos interesantes!», dice Gopi con entusiasmo.
A partir de febrero de 2025, la unidad ofrecerá visitas regulares dirigidas a usuarios potenciales; ¿serás el siguiente? Presta atención a los anuncios, o ponte en contacto con ellos en mif@embl.es.