Este texto está escrito por Júlia Urgel, estudiante de doctorado bajo la supervisión de Ana Janic en el Departamento de Medicina y Ciencias de la vida, Universidad Pompeu Fabra (MELIS-UPF) y Sara Sdelci del Centro de Regulación Genómica (CRG).
Júlia ganó el premio del público en el concurso de divulgación científica Rin4′ con su presentación «Cáncer de pulmón, sin qué no podrías vivir». Aquí nos cuenta más sobre su investigación y lo que la llevó a dedicarse a estudiar el cáncer de pulmón.
Cuando apenas era una adolescente, leí que la mitad de las personas del mundo padecerán cáncer al menos una vez en su vida y que un tercio de los pacientes morirán a causa de él. Este impactante hecho me impulsó a contribuir a la lucha contra el cáncer.
Un año después de tomar esta decisión, mi familia entró en las estadísticas del cáncer. Ver cómo los números se convertían en nombres, rostros y sentimientos me convenció de seguir una carrera en la investigación del cáncer.
Cuando mi familia entró en las estadísticas del cáncer, me convencí del todo de seguir una carrera investigando esta enfermedad.
Júlia Urgel (MELIS-UPF)
Desde entonces, me he ido abriendo camino hasta llegar a desarrollar un proyecto de doctorado en el tipo de cáncer más mortífero y el primer caso de cáncer que se dio en mi entorno más cercano: el cáncer de pulmón.
El cáncer de pulmón es la primera causa de muerte por cáncer a nivel mundial, contando con 1,8 M de muertes en 2022. TP53 y KRAS son los dos genes que más mutan en el cáncer de pulmón y su mutación conjunta conduce a un fenotipo más agresivo con un pronóstico potencialmente peor.
- TP53 es el supresor tumoral más importante, también conocido como el guardián del genoma, lo que significa que regula la división celular impidiendo que las células crezcan y se dividan.
- Por otro lado, KRAS es un oncogén, lo que significa que cuando hay una mutación en él, produce una señal muy intensa y las células crecen sin que nadie se lo ordene, provocando cáncer.
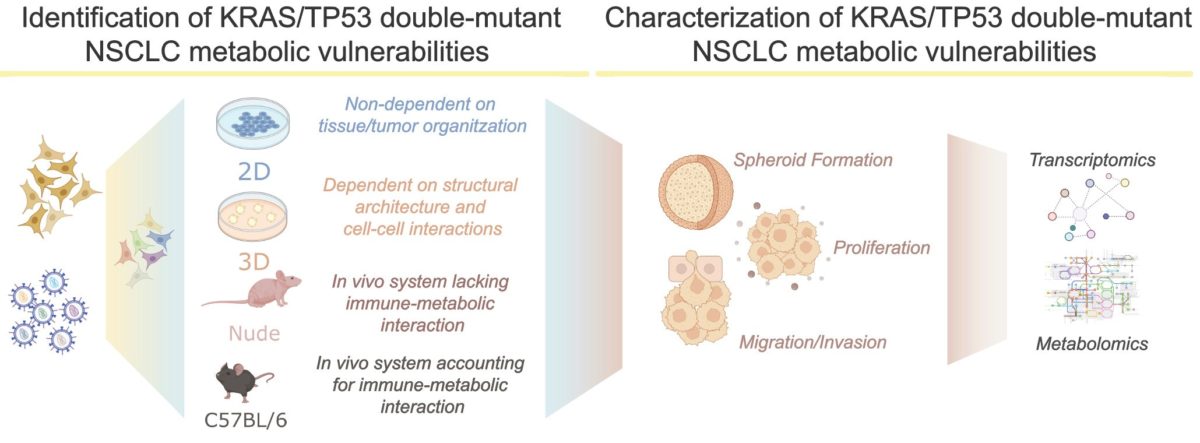
Cuando se estudian por separado, se sabe que los cánceres de pulmón disfuncionales de TP53 o KRAS sufren una profunda adaptación metabólica, diferente de la versión normal (no mutada) de los genes. Sin embargo, aunque constituyen casi el 15% de los casos de cáncer de pulmón de células no pequeñas, se ha descrito muy poco sobre los cambios metabólicos (también conocidos como reajustes metabólicos) que se producen en los tumores que albergan mutaciones en ambos genes. Dado que los reajustes metabólicos son una de las características del cáncer, nuestra hipótesis es que los tumores con doble mutación KRAS/TP53 cambian el metabolismo celular para mantener su proliferación. Por lo tanto, mi futuro proyecto de doctorado se centra en la identificación y caracterización de los genes metabólicos esenciales implicados en la supervivencia de los tumores de pulmón impulsados por la mutación de estos dos genes. Resumiendo:
- TP53 mutante -> conocido por reajustar el metabolismo
- KRAS mutante -> conocido por reajustar el metabolismo
- TP53 + KRAS mutantes -> se desconoce cómo o si cambian el metabolismo
Si nuestra hipótesis es correcta, podríamos decir que ciertos factores metabólicos podrían ser esenciales en los tumores con doble mutación KRAS/TP53, comportándose así como vulnerabilidades metabólicas: genes del metabolismo cuya pérdida promueve la muerte de las células cancerosas que presentan estas mutaciones. Utilizando modelos humanos y de ratón de cáncer de pulmón de células no pequeñas (NSCLC en inglés), pondremos en marcha una serie de experimentos para diseccionar el reordenamiento metabólico que favorece la proliferación de los tumores con doble mutación KRAS/TP53, mediante el cribado genético centrado en el metabolismo.
La información proporcionada por este estudio podría arrojar algo de luz sobre el funcionamiento a nivel molecular de las vías metabólicas en este tipo específico de cáncer de pulmón, lo que podría conducir a nuevas estrategias terapéuticas. Además, nuestros resultados podrían validarse para otros tipos de tumores en los que se ha observado la coexistencia de mutaciones en TP53 y KRAS (como por ejemplo los tumores de páncreas).