D’estudiants de doctorat fins a investigadores principals, estem molt orgullosos de la nostra comunitat al Parc de Recerca Biomèdica de Barcelona (PRBB). Avui volem celebrar els èxits recents d’una científica i un jove científic: Anna Bigas, cap de grup a l’Institut Hospital del Mar d’Investigacions Mèdiques (IMIM), i Akinola Akinbote, estudiant de doctorat al Laboratori Europeu de Biologia Molecular – Barcelona (EMBL Barcelona).
També felicitem a Ana Aldea i a Antonio García de Herreros, tots dos de l’IMIM, pels seus recents nomenaments com a membres de comitès nacionals implicats en la regulació de la investigació clínica i l’avaluació dels investigadors, respectivament.
Reconeixement per dones líders
Anna Bigas, coordinadora del grup d’investigació de Cèl·lules mare i càncer de l’IMIM ha estat escollida una de les millors 100 dones líders d’Espanya, en la categoria d’Acadèmiques, investigadores i pensadores.
Aquest rànquing va ser creat al 2011 per Mujeres & Cia, una revista en línia de referència per a dones professionals que pretén visibilitzar el talent femení i construir una societat basada en la igualtat.
L’Anna Bigas, que és també directora del CIBER de Càncer (CIBERONC), estudia com es generen i renoven les cèl·lules mare que mantenen diferents teixits en condicions fisiològiques. Aquests processos tenen grans semblances amb els que es produeixen en el càncer, de manera que el seu treball se centra principalment en el sistema hematopoètic i el procés de leucèmia.
Destacant veus africanes a STEM
Akinola Akinbote va arribar al laboratori de Kristina Haase a EMBL fa menys d’un any, però ja ha deixat petjada. Recentment va participar al simposi “Africans in STEM” del 2021, on va guanyar un premi per una destacada microxerrada sobre “Enginyeria 3D de microvasculatura humana cardíaca en xip per estudiar la disfunció microvascular coronària“. Parlem amb ell d’aquest simposi i del que significa per a ell.
Primer de tot Akinloa, enhorabona pel premi! Ens pots explicar més sobre el simposi “Africans in STEM”?
Gràcies! Africans in STEM es va fundar a la Universitat de Cambridge per “destacar les contribucions científiques dels africans en ciència, tecnologia, enginyeria i matemàtiques, i per permetre xarxes de suport, intercanvi de idees i col·laboracions”. També estan associats amb la Royal Society of Chemistry i amb Cambridge Africa. Organitzen simposis anuals i altres breus reunions per reunir científics i científiques africanes de tot el món, independentment dels seus àmbits de treball.
Va ser la primera vegada que vas participar?
Sí, aquest era el tercer any que celebraven el simposi, però era la meva primera vegada. Hi havia entre 60 i 100 persones de tot el món; majoritàriament del Regne Unit, però també d’altres països europeus i de diversos països africans, així com alguns dels Estats Units. També hi havia investigadors de tots els nivells, des d’estudiants universitaris fins a professors, tant en l’àmbit acadèmic com industrial.
Per què és important celebrar un simposi específic per a persones d’Àfrica, i què en vas treure?
Ho veig com una via per, en primer lloc, conèixer persones que s’assemblen a mi i que treballen a STEM, on encara som minoritaris; i després, per connectar amb investigadors que tenen una experiència similar a la meva, que provenen d’un context semblant. Com a africà vingut de Nigèria, m’agradaria que la meva investigació ajudés a trobar solucions que siguin rellevants per al meu país, que la tecnologia que estic desenvolupant es pugui utilitzar en altres països del nostre continent. I això necessitarà de gent que hi hagi estat o que hi visqui i sàpiga què és el que cal. Aquest simposi em va donar l’oportunitat de connectar amb diverses persones d’aquest tipus.
M’agradaria que les tecnologies que desenvolupo fossin útils i rellevants també pels països africans; per això és important connectar amb la gent que hi viu.
Akinola Akinbote (EMBL Barcelona)
I quina tecnologia estàs desenvolupant?
Al grup Haase treballem amb teixits in vitro vascularitzats en 3D per al modelatge de malalties, el desenvolupament de medicaments i la medicina regenerativa.
Per superar les limitacions dels sistemes preclínics actuals, com ara els cultius de cèl·lules 2D (als quals els manca l’entorn 3D) o els models animals (que poden presenten diferències específiques entre espècies), calen models in vitro en 3D. Aquests poden ser organoides o dispositius microfluídics; al laboratori Haase ens centrem en aquest últim.
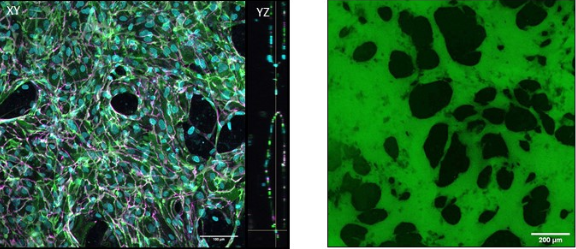
Es tracta de dispositius polimèrics de 4 cm de longitud fets amb PDMS, una mena de silicona, amb un canal al mig. Omplim aquest canal amb cèl·lules primàries humanes barrejades amb un gel de fibrina i les cultivem durant 5-7 dies; en aquests dispositius, i donades les condicions ambientals adequades, es formen microvasos! Aquests vasos són particularment útils quan es formen als nostres dispositius perquè els podem perfondre amb soluts rellevants per entendre les propietats de barrera de la vasculatura, que és la seva funció principal en viu. També podem investigar com s’altera la barrera respecte als canvis en el medi ambient. La Kristina, la cap del laboratori, va desenvolupar aquests models anteriorment al MIT, on els va utilitzar per examinar la salut i la disfunció vascular en el càncer i en la placenta. En el meu cas, estic basant-me en els models anteriors per dissenyar una plataforma de vasculatura in vitro específica per al cor.

Per què necessitem vasos in vitro específics del cor?
Les malalties cardiovasculars causen prop de 18 milions de defuncions anuals, i proves recents han assenyalat que els microvasos més petits del cor són els principals contribuents al desenvolupament patològic de les malalties del cor. La disfunció d’aquests petits vasos cardíacs s’anomena disfunció microvascular coronària (CMD) i, tot i que s’estan desenvolupant diversos models animals, encara ens calen models humans per a comprendre la CMD.
Cal generar vasos realistes específics del cor per comprendre el seu desenvolupament i com es tornen disfuncionals amb el pas del temps. Com que els vasos sanguinis són característics de cada teixit del cos, hem de generar-los a partir del seu teixit d’origen. Per exemple, les cèl·lules endotelials cardíaques han de suportar els batecs constants del cor i regular l’intercanvi de nutrients i gasos en un teixit energèticament exigent per afavorir la contracció muscular del cor.
La construcció d’aquests vasos en un xip també ens permet manipular el microentorn, per exemple, canviant el flux, les condicions hormonals o la concentració d’oxigen. Així, esperem que la generació de vasos específics del cor en aquests dispositius demostri quins són els contribuents clau a la CMD i també ens permeti examinar l’efecte dels tractaments rellevants. Donada la patogènesi poc estudiada de la CMD, juntament amb altres factors que hi contribueixen relacionats amb el sexe i l’edat, és realment important generar models de microvasos cardíacs humans.







