Es ampliamente conocido que las bacterias tienen la capacidad de desarrollar mecanismos de resistencia a los antibióticos. Se trata de un fenómeno natural que, debido al mal uso que se le da a estos medicamentos, se está viendo acelerado.
Los mecanismos de resistencia bacteriana revierten el proceso por el cual el antibiótico altera su estructura o funcionalidad. Según los mecanismos que haya desarrollado cada bacteria, opondrán más o menos resistencia a determinados antibióticos. No obstante, ¿pueden estos microorganismos cambiar su tolerancia a los antibióticos según si conviven o no con otra cepa bacteriana? Un nuevo estudio realizado por Leticia Galera-Laporta y Jordi Garcia-Ojalvo, personal investigador del Departamento de Ciencias Experimentales y de la Salud, Universidad Pompeu Fabra (DCEXS-UPF), lo confirma.
En este trabajo se ha planteado cómo las comunidades con múltiples especies de bacterias — en infecciones y la microbiota, por ejemplo — responden conjuntamente a los antibióticos.
Con este estudio se demuestra la importancia de los mecanismos no genéticos a la hora de desarrollar resistencia a los antibióticos.
Para dar respuesta a esta pregunta, se estudió cómo las bacterias Bacillus subtilis y Escherichia coli responden al antibiótico ampicilina; en solitario, E. coli es sensible al antibiótico, mientras que B. subtilis es resistente. Sin embargo, cuando ambas cepas bacterianas conviven, su respuesta a la ampicilina se invierte. Gracias a un modelo matemático el personal científico pudo ver que lo que realmente cambia es la respuesta colectiva; cuando ambas bacterias conviven, la disponibilidad del medicamento en el medio cambia y, consecuentemente, también lo hace la tolerancia de E. coli y B. subtilis al antibiótico.
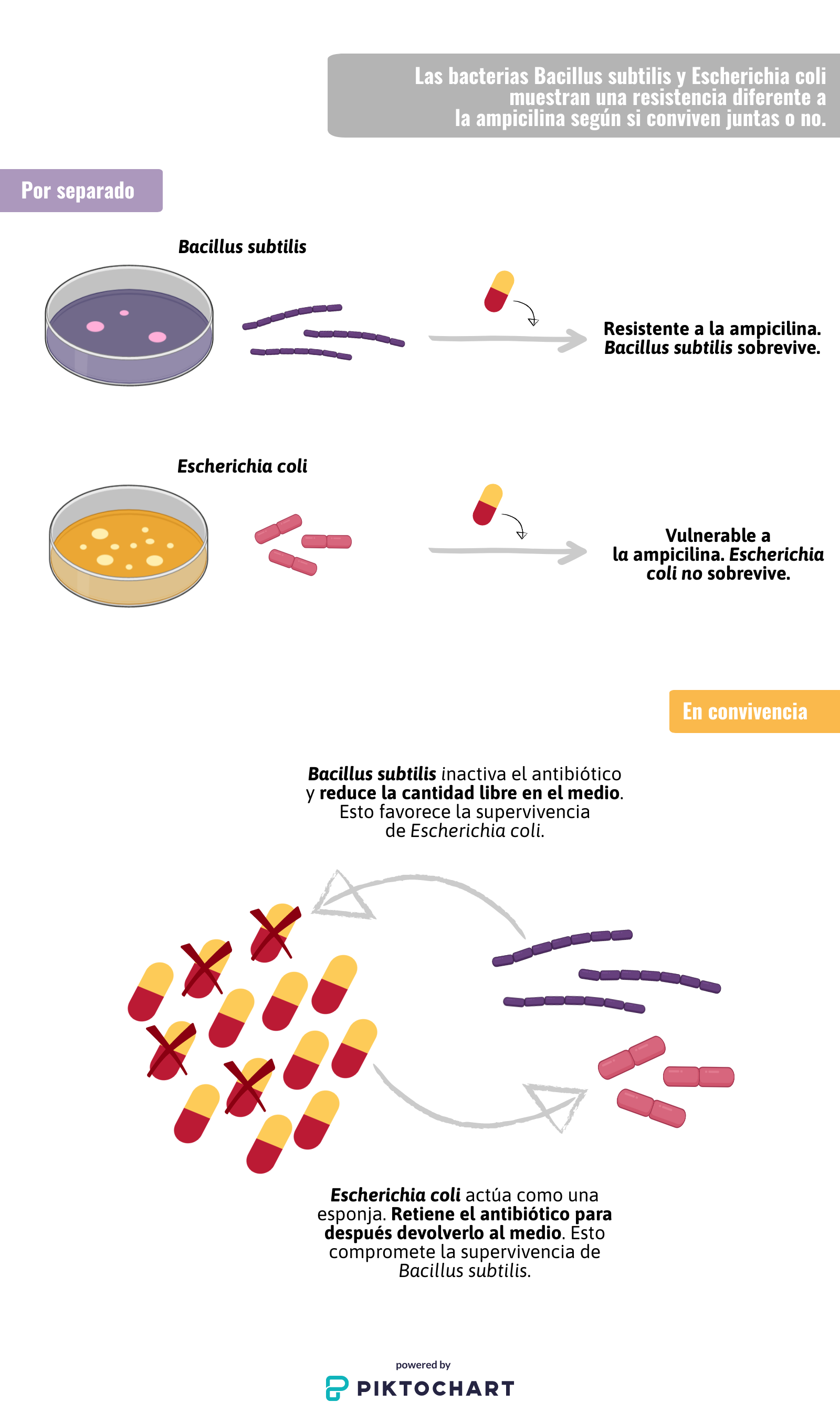
«Es importante considerar el contexto microbiano en el que se encuentran las bacterias para así poder mejorar la información que permita escoger la dosis adecuada de antibiótico en cada caso», concluye Garcia-Ojalvo.
L. Galera-Laporta i J. Garcia-Ojalvo, “Antithetic population response to antibiotics in a polybacterial community”. Science Advances, March 2020. https://doi.org/10.1126/sciadv.aaz5108