La malaria sigue siendo un desafío importante para la salud y la economía global, afectando de manera desproporcionada a los niños y niñas africanos en sus formas más graves. Ahora, un nuevo estudio en colaboración con el grupo dirigido por Maria Bernabeu en el Laboratorio Europeo de Biología Molecular – Barcelona (EMBL Barcelona) ha identificado anticuerpos humanos capaces de reconocer y atacar proteínas clave implicadas en la malaria grave.
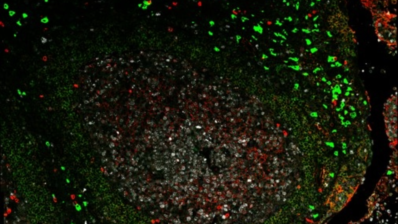
El parásito que causa la enfermedad, Plasmodium falciparum, infecta las células sanguíneas y las modifica para adherirse a las paredes de los microvasos cerebrales. Esta adhesión perjudica el flujo sanguíneo, bloquea pequeños vasos y puede provocar inflamación cerebral y el desarrollo de malaria cerebral.
A medida que crecen, los niños desarrollan inmunidad frente a la malaria, y los adultos rara vez experimentan los efectos letales de la enfermedad. Se cree que esta protección está relacionada con anticuerpos que atacan las proteínas virulentas presentes en la superficie de los glóbulos rojos infectados. Existen unas 60 proteínas de esta familia, llamadas PfEMP1. Sin embargo, la diversidad de variantes de PfEMP1 ha dificultado el desarrollo de una vacuna.
Imitando vasos sanguíneos humanos en el laboratorio
Los equipos investigadores se preguntaron si el sistema inmunitario humano podría generar anticuerpos que atacaran todas las variantes de PfEMP1 en circulación. Un equipo de la Universidad de Texas identificó dos anticuerpos prometedores que se unen a una región específica de PfEMP1 que interactúa con los receptores EPCR, proteínas críticas en las superficies de los glóbulos rojos donde se adhieren las proteínas virulentas del parásito.
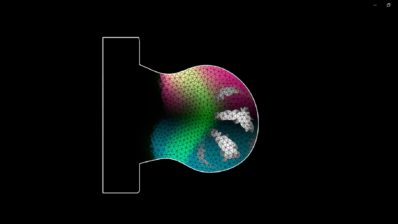
Probar estos anticuerpos en organismos modelo tradicionales era imposible, ya que el parásito solo infecta a humanos y los modelos animales no expresan PfEMP1. Así que hasta ahora, los estudios de eficacia solo pueden realizarse in vitro. Por eso las investigadoras utilizaron tecnología de órganos-en-chip. Crearon una red 3D de vasos sanguíneos humanos en una placa para irrigarla con sangre infectada con malaria y observar la acción de los anticuerpos. Ambos anticuerpos fueron capaces de evitar la acumulación de células infectadas, lo que sugiere que podrían ayudar a prevenir los bloqueos que provocan los síntomas graves de la malaria.
“Introdujimos los dos anticuerpos en el sistema vascular y nos impresionó lo bien que evitaban que las células sanguíneas infectadas se adhirieran a los vasos. Fue sorprendente ver la inhibición claramente a simple vista”.
Viola Introini, co-primera autora del estudio (EMBL Barcelona)
Preguntando a Bernabeu si estos anticuerpos podrían ser útiles contra la malaria en general, responde que están principalmente dirigidos a prevenir la enfermedad grave. Actualmente, hay dos vacunas contra la malaria disponibles y recomendadas por la OMS que atacan al parásito en el hígado, antes de que llegue a la sangre y provoque síntomas graves. Sin embargo, no son completamente efectivas. Existen otras vacunas en ensayos clínicos que son bastante prometedoras. No obstante, dado que el parásito de la malaria es tan complejo y variable, podría ser necesario usar una estrategia combinada que debilite múltiples puntos del ciclo de vida de la malaria.
Un camino complejo por delante
Los investigadores e investigadoras reconocen que trasladar estos hallazgos a tratamientos reales requiere más pasos. «Lo que vemos en estos microvasos de órganos-en-chip es un buen punto de partida, pero queda mucho trabajo por hacer. En este estudio probamos condiciones básicas. Los trabajos futuros incluirán simular inflamación y fiebre, que son críticas durante la malaria grave», explica Bernabeu.
Por ahora, los estudios de eficacia dependen de modelos in vitro, pero el equipo planea ampliar sus esfuerzos de detección para identificar más anticuerpos capaces de atacar otras clases de PfEMP1 que causan enfermedades graves. Incluso podría ser posible, en algún momento, alimentar toda esta información en modelos de IA para diseñar los anticuerpos más eficientes.
El estudio ha sido altamente colaborativo, con contribuciones clave de diferentes grupos que han sido esenciales para el éxito del proyecto. Desde expertos en immunología de la Universidad de Texas que desarrollaron nuevas herramientas de purificación de anticuerpos de donantes, pasando por la biología estructural realizada en San Diego (Scripps Research Institute) o los estudios de cryo-EM y de unión proteína-proteína que se hicieron en Copenhague (Universidad de Copenhague) y Seattle (Fred Hutchinson Cancer Center), hasta el equipo liderado por Bernabeu en el PRBB, donde se diseñaron y probaron los chips de microvasos sanguíneos.
Todos los equipos participantes son conscientes de las amplias implicaciones de su trabajo. Con la carga de la malaria concentrada en zonas de pocos recursos, la accesibilidad y la asequibilidad de los tratamientos son prioritarias. «Si nuestros estudios continúan teniendo éxito, será esencial garantizar que cualquier tratamiento o estrategia preventiva resultante sea accesible para todos«, concluye la líder del grupo.
Reyes, R.A., Raghavan, S.S.R., Hurlburt, N.K. et al. Broadly inhibitory antibodies to severe malaria virulence proteins. Nature 636, 182–189 (2024). https://doi: 10.1038/s41586-024-08220-3