Les condicions en les que un individu ingressa a la Unitat de Cures Intensives (UCI) d’un hospital són crítiques. El pacient sol trobar-se en tal estat que és incapaç de respirar per ell mateix. Si volem salvar la seva vida, és indispensable que sigui sotmès a ventilació mecànica. No obstant, el seu ús, limitat a mantenir amb vida a l’individu crític, no està exempt de riscos.
Recentment, un estudi dirigit per metges de l’Hospital del Mar i investigadors de l’Institut Hospital del Mar d’Investigacions Mèdiques (IMIM) ha destacat que promoure estratègies de ventilació mecànica que permetin treballar la musculatura respiratòria dels pacients ingressats a l’UCI disminueix el dany que pateixen i podria facilitar la seva recuperació.
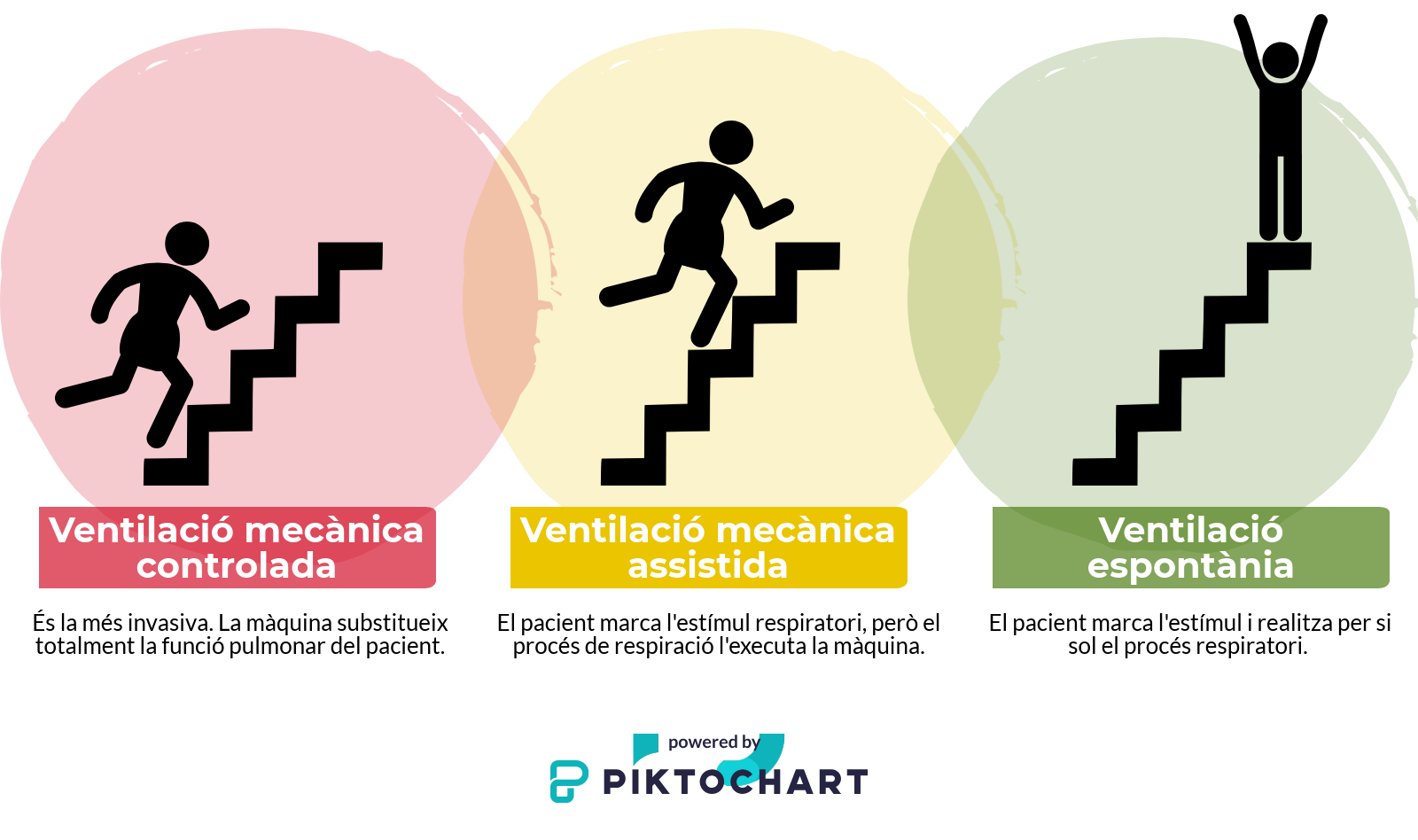
Existeixen tres tipus diferents de ventilació mecànica:
- Ventilació mecànica controlada: és la més invasiva. La màquina substitueix totalment la funció respiratòria del pacient.
- Ventilació mecànica assistida: el pacient marca l’estímul respiratori, però el procés respiratori l’executa la màquina.
- Ventilació espontània: el pacient marca l’estímul i realitza per si sol el procés respiratori.
Els metges de les Unitats de Cures Intensives (UCI) dels hospitals sempre intentaran retirar la ventilació artificial tan aviat com sigui possible. L’objectiu de la retirada és que acabi sent el propi pacient qui torni a respirar per ell mateix i evitar alguns dels problemes que poden sorgir a partir de la ventilació mecànica.
La Dra. Judith Marín, primera autora de l’article, ens explica en aquesta entrevista com ella i el seu equip ha arribat fins aquí i cap a on s’enfocarà la recerca en aquest camp a partir d’ara.

Per què és important estudiar la disfunció muscular en pacients crítics?
Durant molts anys, l’objectiu prioritari dels metges intensivistes ha estat salvar la vida dels pacients. Això ens portava a ser molt invasius en l’ingrés dels pacients, descuidant aspectes tan importants com la disfunció muscular que pateixen rere una estada a l’UCI. A dia d’avui sabem que és aquesta disfunció muscular el que condiciona una pitjor qualitat de vida un cop sobreviuen.
És per això que l’estudi d’aquest camp és important, a l’igual que la implementació de les eines que tenim per avaluar i tractar la disfunció muscular i evitar al màxim que condicioni el dia a dia de l’individu un cop es reincorpori de nou a la seva vida.
Què s’entén per ventilació mecànica?
Quan un pacient pateix una insuficiència respiratòria molt greu o es troba en un nivell de consciència que no el permet respirar per si mateix, hem de posar al seu abast dispositius que supleixin la seva funció respiratòria. Aquests dispositius poden ser no invasius o invasius. El nostre estudi s’ha enfocat en la ventilació mecànica invasiva.
En el cas de la ventilació mecànica, els pacients estan intubats i connectats a una màquina. Segons com fem funcionar la màquina, parlarem de ventilació mecànica controlada, assistida o espontània.
Segons la modalitat de ventilació mecànica que s’utilitzi, s’estarà induint un grau de disfunció diferent en el pacient. La ventilació mecànica controlada seria la modalitat més perjudicial.
Quina és la troballa del vostre estudi respecte els tipus de ventilacions mecàniques?
Es tracta del primer estudi en humans que demostra que, segons la modalitat que s’utilitzi a l’hora d’assistir la respiració dels pacients, estarem induint un grau de disfunció diferent. Com més deixem treballar la musculatura respiratòria del pacient, millor.
En aquesta línia, hem vist que la modalitat més perjudicial és la ventilació mecànica controlada i que, per tant, l’hauríem d’evitar al màxim. Si deixem treballar la musculatura respiratòria dels pacients tan aviat com sigui possible, acurtarem el període de ventilació mecànica i, conseqüentment, els dies d’ingrés a l’UCI.
Com heu demostrat que la ventilació mecànica controlada és la més perjudicial?
A la literatura, els estudis que trobem que relacionen el dany de la musculatura respiratòria amb els mecanismes de ventilació mecànica s’han dut a terme a partir de mostres de donants d’òrgans. No se solen utilitzar biòpsies de diafragma de pacients ingressats a l’UCI i sotmesos a ventilació mecànica ja que, degut a l’estat crític d’aquests individus, el procediment és complicat i poc recomanat.
La novetat de la nostra recerca és la incorporació d’un nou tipus de donant: el Maastricht III. Fins el moment, només s’estudiaven donants per mort encefàlica, és a dir, donants que havien patit una injuria severa a nivell del Sistema Nerviós Central i que, per tant, no podien exercitar el seu diafragma. Aquests donants són sotmesos a ventilació mecànica controlada.
Els donants en asistòlia controlada tipus Maasctricht III també han patit una injuria a nivell del Sistema Nerviós Central però, a diferència dels primers, no han arribat a mort encefàlica, de manera que romanen en coma o estat vegetatiu. Aquests individus sí poden tenir estímuls respiratoris i, per tant, exercitar el seu diafragma. Així doncs, els Maastricht III poden estar sotmesos a ventilació mecànica assistida.
A l’estudi s’ha vist com, a partir de 100 hores d’estar sotmesos a ventilació mecànica sense treball de la musculatura respiratòria, els donants comencen a presentar signes d’atrofia i dany muscular. No obstant, se sap que menys hores ja són perjudicials.
Arrel d’analitzar la musculatura respiratòria d’ambdós tipus de donants hem vist com, en comparació amb els Maastricht III, els pacients per mort encefàlica presentaven unes fibres musculars més petites i amb signes d’afectació a nivell histològic.
Ja que l’obtenció de biòpsies en pacients crítics és complicada, es pot analitzar el diafragma d’aquests individus d’una altra manera que no sigui obtenint biòpsies?
Sí, mitjançant ecografies diafragmàtiques dels pacients. Estem veient com el gruix de les fibres musculars que observem mitjançant l’ecografia es correlaciona molt bé amb el que observem en els estudis histològics de les mostres de donants.
Volem incorporar la realització d’aquestes ecografies de manera sistemàtica per veure com va atrofiant-se el diafragma. Aquest serà el treball que ens permetrà acabar de demostrar que, com més curts siguin els períodes de ventilació mecànica controlada, més curts seran els temps de recuperació.
De quant temps estem parlant a l’hora de guanyar temps en la recuperació?
Això depèn molt del pacient. S’ha d’individualitzar molt. El que sí s’ha vist és que, si un pacient demostra tolerància a la ventilació espontània, cal fer el canvi de ventilació mecànica controlada a espontània l’abans possible ja que, en estudis en animals, s’ha demostrat que la disfunció diafragmàtica associada a la ventilació mecànica es dóna en 6-12 hores.
La disfunció del diafragma apareix en tan sols unes hores d’estar sotmesos a la ventilació mecànica.
A partir d’ara, i gràcies a l’evidència aportada, creus que reduireu el nombre de pacients sotmesos a ventilació mecànica controlada?
El que podem disminuir no és tant el nombre de pacients que necessiten la ventilació mecànica controlada, sinó el temps que estan sotmesos aquests pacients a aquest tipus de ventilació. I per això necessitem protocol·litzar molts processos, entre ells el de sedació. Molts cops veiem que el temps de ventilació mecànica controlada que requereix la patologia s’allarga per altres factors, com l’excés de sedació. És per això que s’han d’establir nous protocols. Cada vegada tenim més eines i fàrmacs que ens permeten tenir a pacients desperts i tranquils tolerant mecanismes de ventilació mecànica. S’ha de treballar en la mobilització precoç d’aquests individus i millorar el seu estat nutricional. Tot això són estratègies que ens ajuden a fer que els músculs treballin.
Marin-Corral, J., Dot, I., Boguña, M. et al. Structural differences in the diaphragm of patients following controlled vs assisted and spontaneous mechanical ventilation. Intensive Care Med. 2019; 45(4):488-500. doi: 10.1007/s00134-019-05566-5